2. Расчётная часть.
2.1. Определение топочных газов, подаваемых на горение.
В качестве топлива используется природный газ следующего состава [в % (об.)] CH4 – 91,6%; С2Н6 – 1,6%; С3Н8 – 0,8%; С4Н10 – 0,4%; С5Н10 – 0,2%; СО2 – 0,6%; N2 – 4,7%; Н2S – 0,1%.
Теоретическое количество сухого воздуха L0, затрачиваемого на сжигание 1 кг топлива, равно: [4]
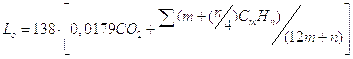 ,
,
где составы горючих газов выражены в объёмных долях. Подставив соответствующие значения, получим:
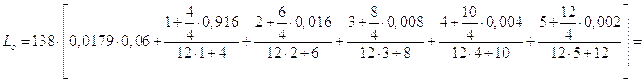
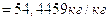
Для определения теплоты сгорания топлива воспользуемся характеристиками горения простых газов [10].
Таблица 1.
Характеристика горения простых газов.
|
Газ |
Реакция |
Тепловой эффект Реакции, кДж/м3 |
|
Водород Метан Этан Пропан Бутан Пентан Сероводород |
H2+0,5CO2=H2O CH4+2O2=CO2+H2O C2H6+3,5O2=2CO2+3H2O C3H8+5O2=3CO2+4H2O C4H10+6,5O2=4CO2+5H2O C5H12+8O2=5CO2+6H2O H2S+1,5O2=SO2+H2O |
108100 358200 637500 912500 1186500 1460800 23100 |
Количество тепла 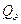 выделившегося при
сжигании 1 м3 газа, равно:
выделившегося при
сжигании 1 м3 газа, равно:
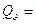
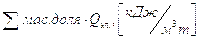 ,
,
где 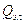 - тепловой эффект
реакции горения простого газа.
- тепловой эффект
реакции горения простого газа.
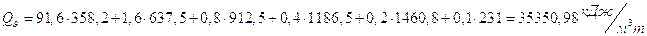
Плотность газообразного топлива ρm равна:
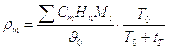 ,
,


 где Mi - молярная масса i - того компонента
топлива, кмоль/кг;
где Mi - молярная масса i - того компонента
топлива, кмоль/кг;
tT - температура топлива, равная 200C;
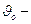 молярный объём,
равный 22,4 м3/кмоль;
молярный объём,
равный 22,4 м3/кмоль;
То - термодинамическая температура, равная 273 К.
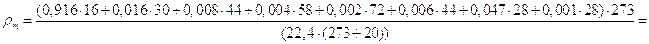
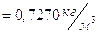 .
.
Количество тепла, выделяющегося при сжигании 1кг топлива:
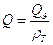
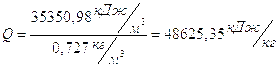
Масса сухого газа, подаваемого в сушильный барабан, в расчёте на 1 кг сжигаемого топлива определяется общим коэффициентом избытка воздуха 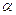 , необходимого для
сжигания топлива и разбавления топочных газов до температуры смеси
, необходимого для
сжигания топлива и разбавления топочных газов до температуры смеси 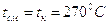 .
.
Значение
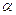 находим из уравнений
материального и теплового балансов. Уравнение материального баланса:
находим из уравнений
материального и теплового балансов. Уравнение материального баланса:
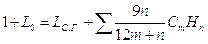 ,
,
где Lс.г. - масса сухих газов, образующихся при сгорании 1 кг топлива; CmHn - массовая доля компонентов, при сгорании которых образуется вода, кг/кг.
Уравнение теплового баланса:
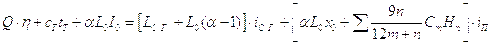 ,
,
где
 - общий коэффициент
полезного действия, учитывающий эффективность работы топки и потери тепла
топкой в окружающую среду, принимаемый равным 0,95;
- общий коэффициент
полезного действия, учитывающий эффективность работы топки и потери тепла
топкой в окружающую среду, принимаемый равным 0,95;
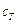 - теплоёмкость
газообразного топлива при
- теплоёмкость
газообразного топлива при 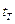 =200С,
равная 1,34 кДж/кг*К;
=200С,
равная 1,34 кДж/кг*К;
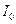 - энтальпия свежего
воздуха, равная 41,53 кДж/кг;
- энтальпия свежего
воздуха, равная 41,53 кДж/кг;
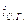 - энтальпия сухих газов
кДж/кг;
- энтальпия сухих газов
кДж/кг; 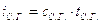 ;
;
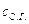 и
и 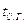 - теплоёмкость и
температура сухих газов;
- теплоёмкость и
температура сухих газов;
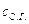 = 1,0416кДж/кг
= 1,0416кДж/кг К,
К, 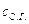 = 2700С;
= 2700С;
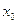 - влагосодержание
свежего воздуха, ( 0,001кг/кг сухого воздуха), при температуре tо= 18 оС и
относительной влажности
- влагосодержание
свежего воздуха, ( 0,001кг/кг сухого воздуха), при температуре tо= 18 оС и
относительной влажности 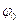 =
78%;
=
78%;
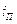 - энтальпия водяных
паров, кДж/кг;
- энтальпия водяных
паров, кДж/кг;
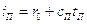 ;
;
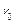 - теплота испарения воды
при температуре 0 оС, равная 2493,1 кДж/кг;
- теплота испарения воды
при температуре 0 оС, равная 2493,1 кДж/кг;
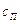 - средняя теплоёмкость
водяных паров, равная 1,97 кДж/(кг
- средняя теплоёмкость
водяных паров, равная 1,97 кДж/(кг К);
К);
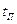 - температура
водяных паров
- температура
водяных паров 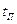 = 270 оС.
= 270 оС.
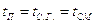 .
.
Решая совместно два уравнения, получим:
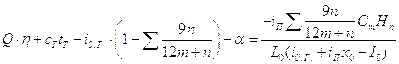 (7)
Пересчитаем компоненты топлива, при сгорании которых образуется
вода, из объемных долей в массовые:
(7)
Пересчитаем компоненты топлива, при сгорании которых образуется
вода, из объемных долей в массовые:
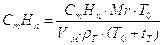 ,
,
где, CmHn - объёмная доля компонента в смеси;
Vм - молярный объём, равный 22,4 моль/л;
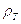 - плотность
газообразного топлива;
- плотность
газообразного топлива;
То - абсолютная температура;
tТ - начальная температура топлива, °С.
СН4 = 0,916 16
16 273/22,4
273/22,4 0,727(273+20)= 0,8385;
0,727(273+20)= 0,8385;
С2Н6
= 0,016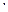 30
30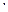 273/22,4
273/22,4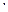 0,727(273+20)=
0,0275;
0,727(273+20)=
0,0275;
С3Н8
= 0,008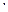 44
44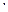 273/22,4
273/22,4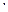 0,727(273+20)=
0,0201;
0,727(273+20)=
0,0201;
С4Н10
= 0,004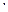 58
58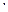 273/22,4
273/22,4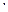 0,727(273+20)=
0,0133;
0,727(273+20)=
0,0133;
С5Н12
= 0,002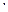 72
72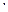 273/22,4
273/22,4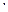 0,727(273+20)=
0,0082;
0,727(273+20)=
0,0082;
Н2S = 0,001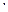 34
34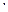 273/22,4
273/22,4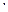 0,727(273+20)=
0,0019.
0,727(273+20)=
0,0019.
Количество влаги, выделяющейся при сгорании 1 кг топлива, равно:
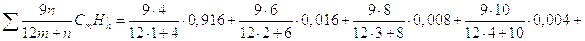
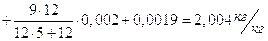 ;
;
Коэффициент избытка воздуха:
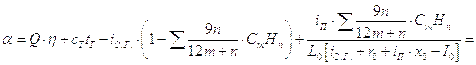
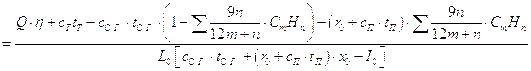 ,
,
где Q - количество тепла, выделяющееся при сжигании 1 кг топлива.
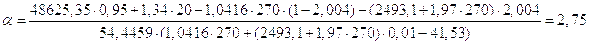
Общая удельная масса сухих газов, получаемых при сжигании 1 кг топлива и набавлении топочных газов воздухом до температуры смеси 270oC равна:
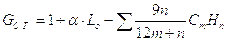 (8)
(8)
Удельная масса водяных паров в газовой смеси при сжигании 1 кг топлива:
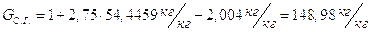
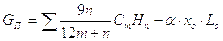 (9)
(9)
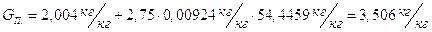
Влагосодержание газов на входе в сушилку x1 на 1 кг сухого воздуха равно:
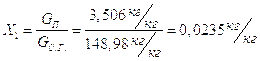
Энтальпия газов на входе в сушилку:
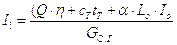
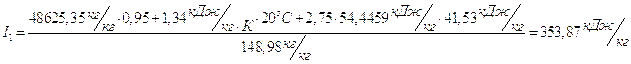














 (zip - application/zip)
(zip - application/zip)