Министерство образования и науки РФ
ФГАОУ БПО «Южный Федеральный Университет»
Академия психологии и педагогики
Кафедра технологии и профессионально-педагогического образования
Реферат на тему
«Основы теории сплавов»
Выполнила: Таратынова Анна Александровна
студентка 1 курса,12 группы
очной формы обучения
профиля «Логистическо-технический сервис
автомобильного транспорта»
Руководитель: Морозова Ольга Николаевна
Ростов-на-Дону
2016
Введение
Общая тенденция развития современной техники и технологии характеризуется стремлением использовать такие конструкционные материалы, которые могли бы обеспечивать достаточную работоспособность изделий не только при нормальных условиях, но и при повышенных скоростях и нагрузках, в условиях космического вакуума, при сверхвысоких и сверхнизких температурах, а также не изменять своей структуры и свойств при длительной работе. Кроме того, машиностроению необходимы сверхлёгкие, высокоупругие, звукопоглощающие и звукопроводящие, теплопроводные и теплозащитные материалы.
Чистые металлы в природе практически не встречаются и в большинстве случаев этими свойствами не обладают, а при получении их из руд к ним всегда примешиваются различные сопутствующие элементы. Получение чистых металлов процесс технологически сложный, требующий больших трудовых и энергетических затрат. К тому же и свойства металлов, особенно прочностные, всегда будут ниже, чем у сплавов.
В качестве же конструкционных материалов применяют в основном металлические сплавы, состоящие из двух и более элементов
Однако нужно иметь в виду, что и чистые металлы имеют применение (электропровода, паяльники, теплообменники, атомная и электронная промышленности).
Понятие сплавов и их характеристика
Под сплавом понимают вещество, полученное сплавлением двух и более химических элементов. Сплав, приготовленный преимущественно из металлических элементов и обладающий металлическими свойствами, называется металлическим сплавом. Сплавы из двух элементов называются двойными или бинарными, из трех и более – многокомпонентными. Примерами бинарных сплавов являются: алюминий – кремний, золото – серебро, медь – цинк, свинец – сурьма. Многокомпонентные сплавы – это чугун, сталь, дюралюминий, состоящие из пяти, шести и более элементов. В каждом сплаве различают компоненты и фазы. Компоненты в данном случае – это химические элементы сплава. Так, для стали компонентами будут железо, углерод, кремний, марганец, сера и фосфор. Фазы – это однородные части сплава, отделенные от других частей поверхностью раздела. Совокупность находящихся в состоянии равновесия фаз определяет систему сплавов. Фаза может быть жидкой и твердой, но обязательно однородной по химическому составу и свойствам. В сплавах могут образовываться следующие фазы: жидкие растворы, твердые растворы и химические соединения. Твердыми растворами называют фазы, в которых один из компонентов сплава сохраняет свою кристаллическую решетку, а другой располагается в ней. Например, алюминий может растворяться в меди до 5,5 %, а цинк в меди до 39 % без изменения кристаллической решетки меди. Такая растворимость называется ограниченной в отличие от неограниченной. Примером неограниченной растворимости являются твердые растворы золота и серебра, никеля и меди. Если компоненты сплава образуют химическое соединение, то кристаллическая решетка соединения и свойства будут значительно отличаться от решеток и свойств исходных компонентов.
Например, двойной сплав медь – алюминий, образующий химическое соединение типа CuAl2, будет иметь твердость, равную НВ = 400 кг/мм2, в то время как твердость алюминия НВ = 20 кг/мм2, а меди НВ = 35 кг/мм2. Студенты должны знать о большом разнообразии применяемых в промышленности металлических сплавов с различными физико-механическими свойствами. Большинство сплавов получают совместным плавлением их компонентов, однако их можно получить также с помощью порошковой металлургии, электролиза, конденсации из парообразного состояния.
Атомное строение двойных сплавов
Естественно, что строение металлических сплавов будет отличаться от строения чистых металлов. Это отличие будет зависеть от того, в какие взаимодействия вступают компоненты двойного сплава. В зависимости от природы компонентов сплава их строение может образовывать: а) механическую смесь компонентов; б) твердый раствор компонентов (замещение или внедрение); в) химическое соединение. Механическая смесь двух компонентов А и В образуется тогда, когда эти компоненты не растворяются в твердом состоянии и не образуют химическое соединение. Строение такого сплава будет состоять из кристаллов А и В, отчетливо выявленных из микро- структуры (рис. 11).
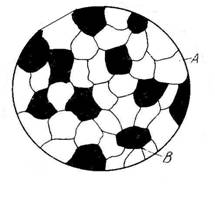
Рис. 11. Схема микроструктуры сплава (механическая смесь)
Твердые растворы представляют собой однофазные сплавы переменного химического состава, в которых сохраняется кристаллическая решетка одного из компонентов (растворителя), а атомы растворенного компонента равномерно располагаются в ней, изменяя ее первоначальные параметры (рис. 12).
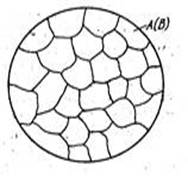
Рис. 12. Схема микроструктуры твердого сплава
Атомы растворяющегося металла или замещают в кристаллической решетке часть атомов растворителя (твердый раствор замещения), или размещаются между атомами металла растворителя (твердый раствор внедрения), при этом размеры решетки возрастают (рис. 13). По данным металло- графического анализа такие сплавы, как и чистый металл, имеет однородные зерна. Способность к образованию твердых растворов присуща не только чистым металлам, но и химическим соединениям типа АnВm. В этих случаях сохраня- ется решетка АnВm, но избыточное количество атомов, например, ато- мов В, растворяется, заменяя в решетке какое-то количество атомов А. Это может привести к тому, что отдельные узлы в решетке окажут- ся не занятыми атомами (будут пустыми).
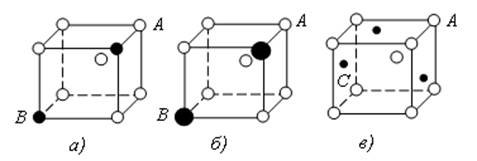
Рис. 13. Кристаллические решетки: а – чистый металл; б – твердый раствор замещения; в – твердый раствор внедрения
Твердые растворы на базе химических соединений, образование которых сопровождается появлением пустых мест в узлах решетки, называются растворами вычитания. Если компоненты сплава А и В образуют химическое соединение типа АnВm, то кристаллическая решетка соединения будет значительно отличаться от решеток его компонентов. Свойства соединения также резко отличаются от свойств исходных компонентов .
Диаграммы состояния двойных сплавов и их характеристика
Результаты исследования плавления и кристаллизации двойных сплавов принято излагать графически в виде диаграмм состояния сплавов. Диаграммы строят в координатах «температура – концентрация» компонентов в процентах. Для построения диаграмм используют термический анализ сплавов при различных концентрациях компонентов. Таким образом, диаграмма состояния двойных сплавов представляет собой графическое изображение состояния сплавов в зависимости от температуры (а) и концентрации компонентов (б). В качестве примера рассмотрим диаграмму состояния «медь – никель» (рис. 15).
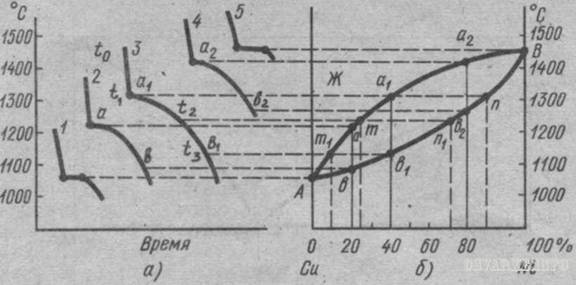
Все сплавы при любой концентрации и при любой температуре, находящиеся выше линии ликвидус* , будут находиться в жидком со- стоянии, ниже линии солидус** – в твердом, между линиями ликвидус и солидус – в жидком и твердом состояниях. Металловедами изучены практически все известные двойные металлические сплавы и представлены в виде диаграмм состояния четырех типов. I тип – диаграмма состояния для сплавов, образующих металлические смеси из чистых металлов. На этом типе диаграмм представлены двойные сплавы, оба компонента которых в жидком состоянии неограниченно растворимы, а в твердом состоянии нерастворимы и образуют структурную механическую смесь компонентов. Примером такой диаграммы состояния I типа может быть сплав «свинец – сурьма».
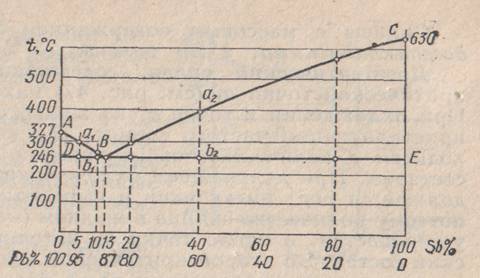
Диаграммы состояния II типа характеризуют системы, компоненты которых полностью растворяются как в жидком, так и в твердом состоянии. Примером служит рассмотренная выше система сплавов «медь – никель».
К диаграммам состояния двойных сплавов III типа относятся сплавы, оба компонента которых неограниченно растворимы в жид- ком состоянии, ограничено в твердом состоянии и не образуют химических соединений. В качестве примера можно привести сплав «медь – серебро» (рис. 17).
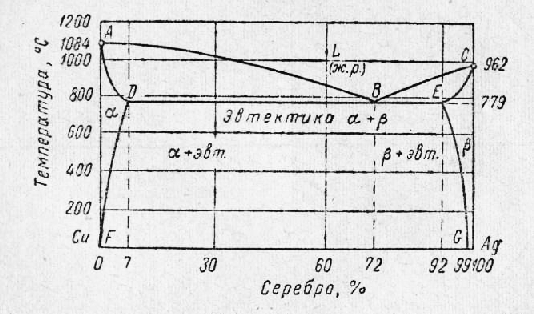
Рис. 17. Диаграмма состояния сплава «медь – серебро»
Диаграмма состояния двойных сплавов IV типа характеризует сплавы, обладающие полной растворимостью в жидком состоянии, нерастворимые в твердом состоянии и образующие устойчивые химические соединения компонентов. Такими сплавами могут быть «магний – кальций», «магний – олово», «железо – углерод» (Fe2C). Элементы образуют химическое соединение всегда в строго определенном массовом соотношении. Поэтому все химические соединения можно выразить формулами типа АnВm, где А и В – элементы, m и n – массовое количество элементов, которое всегда выражается простыми цифрами. Обычно химические соединения образуют сложные кристаллические решетки и обладают высокими показателями твердости, прочности, но в то же время большой хрупкостью. Когда необходима повышенная твердость износостойкости детали, в сплав вводят элементы, которые могут образовывать химические соединения. Представим этот тип диаграмм для сплавов «магний – кальций» (Mg – Ca) (рис. 18).
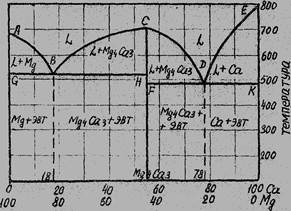
Рис. 18. Диаграмма состояний сплава «магний – кальций»
Химическое соединение Mg4Ca3 можно рассматривать как новый, третий компонент, который делит диаграмму состояния Mg – Са на две диаграммы типа I: Mg – Mg4Ca3 и Mg4Ca3 – Са; каждая из них по- добна системе «свинец – сурьма». Для первой линия ABC – ликвидус, линия FВG – солидус. По линии АВ начинается выпадение кристаллов Mg; по линии ВС – выпадение кристаллов соединения Mg4Ca3. В точке В одновременно кристаллизуются Mg и Mg4Ca3, образуя эвтектику. Доэвтектические сплавы этой системы представляют собой смесь кристаллов магния и эвтетики, а заэвтетические – смесь кристаллов соединения Mg4Ca3 и эвтетики. По аналогии можно сделать анализ и второй диаграммы состояния Mg4Ca3 – Са.
Взаимная связь между диаграммами состояния и свойствами сплавов
Изучив диаграммы состояния двойных сплавов, отметим, что с их помощью можно определить температуру плавления и кристаллизации конкретного сплава, его структуру, не проводя никаких испытаний. В то же время структура сплава, химический состав определяют его механические и технологические свойства. Метод изучения измерения свойств в зависимости от изменения состава и построения диаграммы «состав – свойство» был положен Н.С. Курнаковым в основу разработанного им физико-химического анализа сплавов. В настоящее время этот анализ является одним из основных методов получения новых сплавов с заранее заданными свойствами (рис. 19). При образовании механической смеси на диаграмме а свойства сплава изменяются по линейному закону. Значения свойств сплава находятся в интервале между свойствами чистых компонентов. При образовании неограниченных твердых растворов свойства сплавов изменяются по криволинейной зависимости и достигают максимума примерно при равном количестве компонента А и В (диаграмма б). При образовании ограниченных твердых растворов (диаграмма в) свойства в интервале концентраций, отвечающих однофазным твердым растворам, изменяются по криволинейному, а в двухфазной области диаграммы по прямолинейному закону.
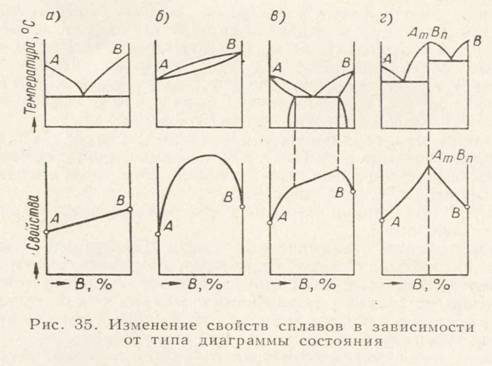
Концентрация отвечает максимуму или минимуму свойств сплавов (диаграмма г). На диаграммах состав – свойства сплавов линии под номером 1 характеризуют прочность, твердость, а под номером 2 – пластичность, электропроводность.
Заключение













 (zip - application/zip)
(zip - application/zip)