Тема: Химия и патохимия водно-электролитного обмена.
Содержание:
1. Водный обмен. Обмен воды и электролитов в организме.
2. Понятие об осмотическом давлении в тканях. Осмолярность плазмы и мочи.
3. Минеральный обмен. Роль минеральных веществ в жизнедеятельности организма.
4. Распределение в организме, регуляция и клинико-диагностическое значение минеральных веществ.
5. Механизм поддержания внеклеточного объёма жидкости и внеклеточного ионного состава, их нарушения.
Водный обмен
— совокупность процессов всасывания воды, введенной в организм при питье и с пищевыми продуктами,
распределения ее в организме, образования воды при окислении жиров, углеводов и белков в тканях и
выделения воды почками, легкими, кожей и кишечником. Водный обмен — составная
часть общего обмена веществ организма.
Общее содержание воды во взрослом организме составляет 65—70% (у эмбрионов достигает 97%), при
этом вода находится в
свободном и связанном состоянии. Свободная вода легко переходит из клеток во
внеклеточное пространство, плазму крови, лимфу и обратно; связанная вода прочно
удерживается главным образом белками. В здоровом организме взрослого человека
сохраняется состояние водного равновесия (баланс), т. е. количество воды,
потребляемой и образующейся в организме, равно количеству выделяемой воды.
Общее количество потребляемой при питье и с пищевыми продуктами воды равно
2000—2500 мл, в том числе при питье — 1200—1500 мл в сутки. Выделение воды
происходит главным образом через почки (50—60%), остальная часть
выделяется через кожу, легкие и кишечник. Водный обмен регулируется центральной
нервной системой и гормонами. Нарушение функции регуляторных систем может
вызвать тяжелые нарушения водного обмена и водного баланса, например отеки при
диабетах, нефритах и др.
Обмен воды и электролитов
Водно-электролитный обмен это совокупность процессов поступления, всасывания, распределения и выделения из организма воды и электролитов. Он обеспечивает постоянство ионного состава, кислотно-основного равновесия и объема жидкостей внутренней среды организма. Ведущую роль в нем играет вода.
Функции воды:
· внутренняя среда организма;
· структурная;
· всасывание и транспорт веществ;
· участие в биохимических реакциях (гидролиз, диссоциация, гидратация, дегидратация);
· конечный продукт обмена;
· выделение при участии почек конечных продуктов обмена.
Содержание воды в организме варьирует в зависимости от органов и тканей. Мозг – 70-84%, почки – 82%, сердце и легкие – 79%, мышцы – 76%, кожа – 72%, печень – 70%, костная ткань – 10%.
Вода, которая поступает алиментарным (с пищей) путем называется экзогенной, а образовавшаяся в качестве продукта биохимических превращений – эндогенной.
Даже незначительные нарушения солевого состава плазмы могут оказаться губительными для многих тканей, прежде всего для клеток самой крови. Суммарная концентрация минеральных солей, белков, глюкозы, мочевины и других веществ, растворенных в плазме, создает осмотическое давление.
Явление осмоса возникает везде, где имеются два раствора различной концентрации, разделенные полупроницаемой мембраной, через которую легко проходит растворитель (вода), но не проходят молекулы растворенного вещества. В этих условиях растворитель движется в сторону раствора с большей концентрацией растворенного вещества. Одностороннюю диффузию воды через полупроницаемую перегородку называют осмосом.
 Осмотическое
давление плазмы в основном создается неорганическими солями, поскольку
концентрация сахара, белков, мочевины и др. органических веществ в плазме
невелика. Осмотическое давление обеспечивает в организме обмен воды между
кровью и тканями.
Осмотическое
давление плазмы в основном создается неорганическими солями, поскольку
концентрация сахара, белков, мочевины и др. органических веществ в плазме
невелика. Осмотическое давление обеспечивает в организме обмен воды между
кровью и тканями.
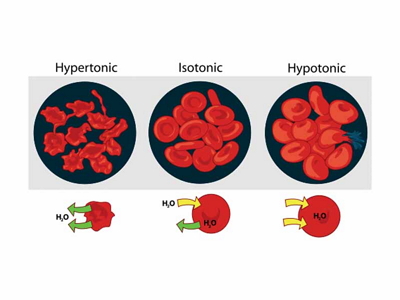
Солевой раствор, имеющий такое же осмотическое давление, как плазма крови, называют изотоническим раствором. Для человека изотоничен 0,9% раствор поваренной соли, а для лягушки – 0,6% раствор этой же соли. Солевой раствор, осмотическое давление которого выше, чем осмотическое давление плазмы крови, называют гипертоническим; если осмотическое давление раствора ниже, чем в плазме крови, такой раствор называют гипотоническим.
Поскольку растворитель движется всегда в сторону более высокого осмотического давления, то при погружении эритроцитов в гипотонический раствор, по законам осмоса, вода интенсивно начинает проникать внутрь клеток. Клетки набухают, их оболочки разрываются, и содержимое эритроцитов поступает в раствор. Наблюдается гемолиз. Кровь, в которой эритроциты подверглись гемолизу, становится прозрачной, или, как иногда говорят, лаковой. У человека гемолиз начинается при помещении его эритроцитов в 0,44-0,48% раствор NaCl, а в растворах 0,28-0,32% NaCl уже почти все эритроциты оказываются разрушенными. Если эритроциты попадают в гипертонический раствор, они сморщиваются.
Несмотря на то, что в кровь может поступать разное количество воды и минеральных солей, осмотическое давление крови поддерживается на постоянном уровне. Это достигается благодаря деятельности почек, потовых желез, через которые из организма удаляются вода, соли и другие продукты обмена веществ.
Осмолярность – сумма концентраций катионов анионов и неэлектролитов, т.е. всех кинетически активных частиц в 1л. раствора. Она выражается в миллиосмолях на литр (мосм/л).
Осмоляльность – концентрация тех же частиц, растворенных в килограмме воды, выражающаяся в миллиосмолях на килограмм (мосм/кг).
Показатели осмолярности в норме
Плазма крови – 280-300
СМЖ – 270-290
Моча – 600-1200
Индекс осмолярности – 2,0-3,5
Клиренс свободной воды – (-1,2) – (-3,0) мл/мин
Определение осмолярности помогает:
1. Диагностировать гипер- и гипоосмолярные синдромы
2. Выявлять и целенаправленно лечить гиперосмолярные коматозные состояния и гипоосмолярные гипергидратации.
3. Диагностировать ОПН в раннем периоде.
4. Оценивать эффективность трансфузионно-инфузионно- терапии.
5. Диагностировать острую внутричерепную гипертензию.
Значение осмометрии для ранней диагностики ОПН.
Классические индикаторы ОПН – мочевина и креатинин – повышаются в крови только тогда, когда в патологический процесс вовлечены, более 50% нефронов (на 3-4 день олигурии), поэтому они в ранней диагностике ОПН роли не играют. С учетом патогенеза ОПН, в основе которого лежит преимущественное поражение канальцевого аппарата, для ранней диагностики ОПН важно изучение осмотического концентрирования мочи канальцевым эпителием. В этой связи высокой прогностической ценностью обладает метод определения осмолярности мочи и клиренс свободной воды (КСВ) в максимально ранние сроки у больных с угрозой развития ОПН. Величина осмолярности мочи 350-400 мосм/л является критическим уровнем, предшествующим ОПН, особенно в сочетании с низким выделением мочевины.
КСВ – является чувствительным показателем концентрационной функции почек. В норме он составляет от (-1,2) до (-3) мл/мин. и увеличивается, т.е. сдвигается в положительную сторону, при развитии почечной недостаточности. По увеличению КСВ можно диагностировать ОПН на 24-72 ч. раньше, чем по изменению классически конечных показателей – urea и creat.
КСВ рассчитывается следующим образом: измеряют осмолярность мочи (осм) и плазмы, отношение между которыми называется индексом осмолярности, в норме он равен 2,0-3,5. Затем рассчитывают осмотический клиренс (Сосм) – объем плазмы (в миллилитрах), полностью очищенной от осмотически активных веществ, за 1 мин., по формуле:
Сосм = (Vм x Осм) : Опл
где Vм – скорость мочеотделения, мл/мин.
КСВ – разность между минутным объемом мочи и осмотическим клиренсом
КСВ = Vм – Сосм
Прогрессивное увеличение осмолярности плазмы и низкая осмолярность мочи, а также соответственно значительное снижение индекса осмолярности является одним из показателей поражения паренхимы почек.
Гипоосмолярность, гиперосмолярность
Определение осмолярности – очень сложное лабораторно-диагностическое исследование. Однако, его проведение позволяет вовремя выявить симптомы таких нарушений, как гипоосмолярность, то есть снижение осмолярности плазмы крови, и гиперосмолярность – наоборот, повышение осмолярности. Причиной снижения осмолярности могут послужить различные факторы, например, превышение уровня свободной воды, содержащейся в плазме крови относительно объема растворенных в ней кинетических частиц. Собственно о гипоосмолярности можно говорить уже тогда, когда уровень осмолярности плазмы крови упадет ниже 280 мосм/л. В числе симптомов, появление которых может говорить о таком нарушении как гипоосмолярность, можно обозначить утомляемость, головную боль, тошноту, приводящую к рвоте и снижение аппетита. При развитии нарушения у больного наблюдаются патологические рефлексы, олигурия, бульбарный паралич и угнетение сознания.
Что касается такого нарушения, как гиперосмолярность, она вызывается, как уже было сказано, повышением осмолярности плазмы крови. При этом, критической отметкой является показатель выше 350 мосм,л. Своевременное обнаружение гиперосмолярности имеет особенное значение, поскольку именно это нарушение представляет собой самую частую причину комы при сахарном диабете. Именно геперосмолярность не только может являться для больных сахарным диабетом причиной комы, но и вызывать ее возникновение вследствие лактацидоза или кетоацидоза. Таким образом, наблюдение за уровнем осмолярности плазмы крови действительно имеет огромное значение, поскольку позволяет контролировать стабильное состояние организма и вовремя предотвращать разного рода нарушения.
Минеральный обмен – совокупность процессов всасывания, распределения, усвоения и выделения минеральных веществ, находящихся в организма преимущественно в виде неорганических соединений.
Всего в организме обнаруживается свыше 70 элементов таблицы Д.И. Менделеева, 47 из них присутствуют постоянно и называются биогенными. Минеральные вещества играют важную роль в поддержании кислотно-основного равновесия, осмотического давления, системе свертывания крови, регуляции многочисленных ферментных систем и пр., т.е. имеют решающее значение в создании и поддержании гомеостаза.
По количественному содержанию в организме они делятся на макроэлементы, если их больше чем 0,01 % от массы тела (К, Са, Мg, Na, P, Cl) и микроэлементы (Mn, Zn, Cr, Cu, Fe, Co, Al, Se). Основную часть минеральных веществ организма составляют хлористые, фосфорнокислые и углекислые соли натрия, кальция, калия, магния. Соли в жидкостях организма находятся в частично или полностью диссоциированном виде, поэтому минеральные вещества присутствуют в виде ионов – катионов и анионов.
Функции минеральных веществ:
- пластическая (кальций, фосфор, магний);
- поддержание осмотического давления (калий, натрий, хлор);
- поддержание буферности биологических жидкостей (фосфор, калий, натрий);
- поддержание коллоидных свойств тканей (все элементы);
- детоксикационная (железо в составе цитохрома Р-450, сера в составе глутатиона);
- проведение нервного импульса (натрий, калий);
- участие в ферментативном катализе в качестве кофактора или ингибитора;
- участие в гормональной регуляции (йод, цинк и кобальт входят в состав гормонов).
Промежуточный и конечный обмен минеральных веществ
Поступают минеральные вещества в организм в свободном или связанном виде. Ионы всасываются уже в желудке, основная часть минеральных веществ – в кишечнике путем активного транспорта при участии белков – переносчиков. Из желудочно-кишечного тракта поступают в кровь и лимфу, где связываются со специфическими транспортными белками. Выделяются минеральные вещества главным образом в виде солей и ионов.
С мочой: натрий, калий, кальций, магний, хлор, кобальт, йод, бром, фтор.
С калом: железо, кальций, медь, цинк, марганец, молибден, и тяжелые металлы.
Характеристика отдельных элементов
Натрий – основной катион внеклеточного отдела. Составляет 0.08 % от массы тела. Играет главную роль в поддержании осмотического давления. При отсутствии или ограничении в поступлении натрия в организм его выделение с мочой почти полностью прекращается. Всасывается в верхнем отделе тонкого кишечника при участии белков-переносчиков и требует затраты АТФ. Суточная потребность варьирует в зависимости от водно-солевого обеспечения организма. Депонируется в коже и мышцах. Кишечная потеря натрия происходит при диареях.
1/) участвует в возникновении и поддержании электрохимического потенциала на плазматических мембранах клеток;
2/) регулирует состояние водно-солевого обмена;
3/) участвует в регуляции работы ферментов;
4/) компонент K+ - Na+ насоса.
Хлор – важнейший анион внеклеточного пространства. Составляет 0,06% от массы тела. Большая часть его содержится в желудочном соке. Участвует в поддержании осмотического равновесия. Активирует амилазу и пептидазы. Всасывается в верхних отделах кишечника, выделяется в основном с мочой. Концентрация хлора и натрия обычно изменяются параллельно.
Калий – составляет 0,25% от массы тела. Во внеклеточном пространстве содержится только 2% от общего количества, а остальное - в клетках, где связан с углеводными соединениями. Всасывается на протяжении всего желудочно-кишечного тракта. Часть калия откладывается в печени и коже, а остальная поступает в общий кровоток. Обмен очень быстро протекает в мышцах, кишечнике, почках и печени. В эритроцитах и нервных клетках более медленный обмен калия. Играет ведущую роль в возникновении и проведении нервного импульса. Необходим для синтеза белков (на 1г белка – 20 мг ионов калия), АТФ, гликогена, принимает участие в формировании потенциала покоя. Выделяется в основном с мочой и меньше с калом.
Кальций – внеклеточный катион. Составляет 1,9 % от массы тела. Содержание повышается в период роста или беременности. Функционирует как составная часть опорных тканей или мембран, участвует в проведении нервного импульса и инициации мышечного сокращения, является одним из факторов гемокоагуляции. Обеспечивает целостность мембран (влияет на проницаемость), т. к. способствует плотной упаковке мембранных белков. Кальций ограничено участвует в поддержании осмотического равновесия. Вместе с инсулином активирует проникновение глюкозы в клетки. Всасывается в верхнем отделе кишечника. Степень его усвоения зависит от рН среды (соли кальция в кислой среде нерастворимы). Жиры и фосфаты препятствуют всасыванию кальция. Для полного усвоения из кишечника необходимо наличие активной формы витамина Д3
Большая часть кальция содержится в костной ткани (99%) в составе микрокристаллов карбонатапатита 3Са2(РО4)2 · СаСО3 и гидроксилапатита 3Са2(РО4)2 · СаОН. Общий кальций крови включает три фракции: белоксвязанный, ионизированный и неионозированный (который находится в составе цитрата, фосфата и сульфата).
Магний – составляет 0.05% от массы тела. В клетках его содержится в 10 раз больше, чем во внеклеточной жидкости. Многого магния в мышечной и костной ткани, также в нервной и печеночной. Образует комплексы с АТФ, цитратом, рядом белков.
1/) входит в состав почти 300 ферментов;
2/) комплексы магния с фосфолипидами снижают текучесть клеточных мембран;
3/) участвует в поддержании нормальной температуры тела;
4/) участвует в работе нервно-мышечного аппарата.
Неорганический фосфор - содержится преимущественно в костной ткани. Составляет 1% от массы тела. В плазме крови при физиологических рН фосфор на 80 % представлен двухвалентным и на 20 % одновалентным анионом фосфорной кислоты. Фосфор входит в состав коферментов, нуклеиновых кислот, фосфопротеинов, фосфолипидов. Вместе с кальцием фосфор образует апатиты – основу костной ткани.
Медь входит в состав многих ферментов и биологически активных металлопротеинов. Участвует в синтезе коллагена и эластина. Является компонентом цитохрома с электронтранспортной цепи.
Сера – составляет 0.08%. Поступает в организм в связанном виде в составе АК и сульфат-ионов. Входит в состав желчных кислот и гормонов. В составе глутатиона участвует в биотрансформации ядов.
Железо входит в состав железосодержащих белков и гема гемоглобина, цитохромов, пероксидаз.
Цинк – является кофактором ряда ферментов.
Кобальт входит в состав витамина В12.
Гомеостаз, гомеостазис (homeostasis; греч. homoios подоб¬ный, тот же самый + stasis состояние, неподвижность),— относительное динамическое постоянство внутренней среды (крови, лимфы, тканевой жидкости) и устойчивость основных физиологических функций (кровообращения, дыхания, терморегуляции, обмена веществ и так далее) организма человека и животных. Регуляторные механизмы, поддерживающие физиологическое состояние или свойства клеток, органов и систем целостного организма на оптимальном уровне, называются гомеостатическими.
Живая клетка представляет подвижную, саморегулирующуюся систему. Ее внутренняя организация поддерживается активными процессами, направленными на ограничение, предупреждение или устранение сдвигов, вызываемых различными воздействиями из окружающей и внутренней среды. Способность возвращаться к исходному состоянию после отклонения от некоторого среднего уровня, вызванного тем или иным «возмущающим» фактором, является основным свойством клетки. Многоклеточный организм представляет собой целостную организацию, клеточные элементы которой специализированы для выполнения различных функций. Взаимодействие внутри организма осуществляется сложными регулирующими, координирующими и коррелирующими механизмами с участием нервных, гуморальных, обменных и других факторов. Множество отдельных механизмов, регулирующих внутри- и межклеточные взаимоотношения, оказывает в ряде случаев взаимопротивоположные (антагонистические) воздействия, уравновешивающие друг друга. Это приводит к установлению в организме подвижного физиологического фона (физиологического баланса) и позволяет живой системе поддерживать относительное динамическое постоянство, несмотря на изменения в окружающей среде и сдвиги, возникающие в процессе жизнедеятельности организма.
Механизм поддержания внеклеточного объёма жидкости и внеклеточного ионного cостава, их нарушения
Постоянство объёма и осмолярности внеклеточной жидкости поддерживается регуляторными механизмами, главным эффекторным органом которых являются почки. Повышение осмолярности плазмы крови вследствие потери чистой воды является специфическим раздражителем осморецепторов, заложенных в переднем гипоталамусе. В результате появляется чувство жажды. Жажда – это один из главных и наиболее чувствительных признаков дефицита воды. Наличие жажды показывает, что объём воды во внеклеточном пространстве уменьшен относительно содержания в нём солей. Раздражение осморецепторов гипоталамической области (при повышении осмолярности крови), а также волюмрецепторов левого предсердия (при уменьшении объёма крови) усиливает секрецию вазопрессина (АДГ) супраоптическими и паравентрикулярными ядрами гипоталамуса. Вазопрессин усиливает реабсорбцию воды в дистальных канальцах нефрона через активацию V2 рецепторов эпителия и образования цАМФ, который повышает проницаемость их для воды. Стимулирующий эффект АДГ определяется пермиссивным действием АКТГ аденогипофиза. Это ведёт к уменьшению диуреза, увеличению объёма циркулирующей крови. Кроме того, АДГ суживает артериолы и повышает артериальное давление.
Секреция АДГ может также стимулироваться и не осмотическими факторами, из которых наиболее важен – снижение сосудистого объёма. Стимуляция АДГ при этом возникает вследствие влияния на рецепторы низкого давления (локализованные в предсердиях), так и на рецепторы высокого давления (локализованные в каротидном синусе). Парасимпатическая цепочка связывает эти рецепторы объёма с нейрогипофизом. При этом снижение интраваскулярного объёма стимулирует так называемый центральный механизм высвобождения АДГ. Дополнительными неосмотическими факторами стимуляции АДГ являются также болевой синдром, эмоциональный стресс, β-адренергическая стимуляция. Некоторые лекарственные средства могут стимулировать (никотиновая кислота, наркотики, винкристин, циклофосфамид) или ингибировать (этанол, наркотические аналгетики) секрецию АДГ.
Раздражение рецепторов приводной артерии почек (при уменьшении почечного кровотока, кровопотере) и натриевых рецепторов плотного пятна юкстагломерулярного аппарата (при дефиците натрия) усиливает синтез и освобождение ренина. Под влиянием ренина из ангиотензиногена плазмы крови образуется ангиотензин І. Это вещество ещё не обладает биологической активностью. При прохождении через капилляры лёгких из ангиотензина І под действием конвертирующего фермента эндотелиальных клеток образуется ангиотензин ІІ. В дальнейшем под влиянием ангиотензиназ происходит образование ангиотензина ІІІ. Ангиотензин ІІ оказывает два эффекта: 1) вызывает сокращение гладких мышц артериол, в результате чего происходит их сужение и повышается артериальное давление; 2) действуя на клубочковую зону коры надпочечников, он активирует секрецию альдостерона. Ангиотензин ІІІ обладает только одним действием – увеличивает секрецию альдостерона.
Основные функциональные эффекты альдостерона связаны с его влиянием на почки. Действуя на дистальные извитые канальцы нефронов, альдостерон вызывает: 1) увеличение реабсорбции Na+; 2) увеличение секреции К+; 3) увеличение секреции Н+ (усиливает ацидогенез).
Антидиуретическим и антинатрийурическим механизмам противостоят диуретические и натрийурические. Главными факторами их являются реномодулярные простагландины и атриальный натрийурический фактор (АНФ, атриопептид). АНФ синтезируется в клетках левого предсердия. Он повышает диурез и натрийурез, расслабляет гладкие мышечные волокна сосудов и снижает артериальное давление. Содержание АНФ в левом предсердии и секреция его в кровь увеличивается после избыточного потребления воды и солей, вследствие растяжения предсердий, повышения артериального давления, а также стимуляции a-адренорецепторов и рецепторов вазопрессина. Эти механизмы функционируют постоянно и обеспечивают восстановление водно-электролитного баланса после кровопотери, обезвоживании, в случае избытка воды в организме, а также изменения осмотической концентрации внеклеточной жидкости.
При патологических состояниях может нарушаться интеграция механизмов регуляции водного баланса. Например, при сердечной недостаточности, циррозе печени, нефротическом синдроме сохраняется тенденция к задержке воды и натрия, несмотря на значительное увеличение как объёма внеклеточной жидкости, так и общего содержания натрия и воды. В других ситуациях нарушаются механизмы сохранения воды и натрия, поэтому наблюдается их потеря.
Нарушения водно-электролитного баланса
Потеря воды организмом (дегидратации)
Нарушения водно-солевого обмена делят на обезвоживание (дегидратацию) и задержку воды в организме (гипергидратацию). В зависимости от изменения осмотической концентрации (соотношения воды и электролитов) дегидратацию и гипергидратацию подразделяют на изоосмолярную, гипоосмолярную и гиперосмолярную.
Изоосмолярная дегидратация развивается при эквивалентной потере воды и электролитов. Это наблюдается при полиурии, кишечном токсикозе, острой кровопотере, рвоте, поносе. При этом уменьшение количества тканевой жидкости идёт преимущественно за счёт внеклеточной.
Гипоосмолярная дегидратация характеризуется уменьшением осмотического давления внеклеточной жидкости и наблюдается в случае преимущественной потери солей. Она развивается при потере секретов желудка и кишок (понос, рвота), повышенном потоотделении, если потеря воды возмещается питьём без соли. При этом снижение осмотического давления во внеклеточной среде приводит к переходу воды в клетки, вследствие чего усиливается гиповолемия, сгущение крови и нарушение кровообращения, снижается фильтрационная способность почек, развивается дегидратация клеток (в частности нервных) и нарушение их функции.
Обезвоживание и потеря электролитов приводит к нарушению кислотно-основного равновесия. Так, обезвоживание с потерей хлоридов и ионов Н+ желудочного сока приводит к алкалозу. Снижение панкреатического и кишечного соков, которые содержат больше натрия и гидрокарбонатов, ведёт к ацидозу.
Гиперосмолярная дегидратация развивается при потере воды, в результате чего увеличивается осмотическое давление внеклеточной жидкости. Это наблюдается в тех случаях, когда потеря воды превышает потерю электролитов (прежде всего, натрия), например, при гипервентиляции, профузном потоотделении, потере слюны, а также при поносе, рвоте, полиурии, когда возмещение потери воды недостаточно. При этом наступает уменьшение объёма внеклеточной жидкости и нарастание её осмотичности. Увеличение осмотического давления внеклеточной жидкости ведёт к перемещению воды из клеток. Обезвоживание клеток вызывает мучительное чувство жажды, усиление распада белков, повышение температуры, а иногда – помрачение сознания, кому. Увеличение осмотического давления межклеточной жидкости ведёт к внутриклеточному обезвоживанию и увеличению внутриклеточной концентрации электролитов, что ведёт к нарушению гидратных оболочек белковых молекул. Уменьшается растворимость белков, они осаждаются, что проявляется нарушением их функций. Уменьшение воды в клетках приводит к уменьшению их объёма и к уменьшению активной поверхности клеточных мембран. В результате этого нарушаются функции, связанные с плазматической мембраной – межклеточных взаимодействий, восприятия регуляторных сигналов, миграции и др.
Среди общих нарушений на уровне организма внутриклеточное обезвоживание проявляется расстройствами функции нейронов ЦНС. Это проявляется развитием невыносимой жажды, помрачением сознания, галлюцинациями, нарушениями ритма дыхания. Обезвоживание эндотелиальных клеток ведёт к увеличению промежутков между ними, увеличению проницаемости стенки сосудов. Это может быть причиной выхода из капилляров в ткани белков плазмы крови и её форменных элементов – развиваются геморрагии.
Повышенное выведение воды из организма наблюдается при несахарном диабете. Основным фактором патогенеза несахарного диабета является уменьшение продукции вазопрессина. Причиной несахарного диабета могут быть опухоли, воспалительный процесс, саркоидоз или травма, поражающие нейрогипофиз, ножку гипофиза или ядра гипоталамуса.
Вторая форма болезни – первичная полидипсия психогенного происхождения, которая сопровождается вторичной полиурией.
Третьей формой болезни является нефрогенный несахарный диабет, в основе которого лежит снижение чувствительности почек к вазопрессину. При этом отмечается снижение продукции в эпителии канальцев цАМФ и снижение проницаемости дистальной части канальца нефрона для воды.
Уменьшение содержания воды в жидкой части крови ведёт к ангидремии, гиповолемии и снижению объёма циркулирующей крови. Крайним проявлением внеклеточного обезвоживания является развитие ангидремического шока. Основное значение в его развитии имеют: 1) гиповолемия (уменьшение объёма циркулирующей крови). Она является причиной нарушения общей гемодинамики. Уменьшается минутный объём крови и артериальное давление, что ведёт к развитию циркуляторной гипоксии и метаболического ацидоза. В результате гемодинамических нарушений развивается острая почечная недостаточность: уменьшается фильтрационное давление, развиваются олиго- и анурия, гиперазотемия и уремия; 2) гемоконцентрация (сгущение крови, увеличение её вязкости). Вызывает прежде всего нарушения микроциркуляции, замедляется кровоток в капиллярах, развивается сладж-синдром, истинный капиллярный стаз. Следствием таких расстройств является развитие гипоксии и ацидоза. Гипоксия, ацидоз и интоксикация являются основными факторами, нарушающими функции ЦНС и других жизненноважных органов и приводящими к смерти. Признаки тяжёлой ангидремии и смерть наступают у взрослых после потери 1/3, у детей – 1/5 объёма внеклеточной жидкости.
В защитно-компенсаторных реакциях организма при обезвоживании принимают участие функциональные эффекты симпатоадреналовой системы, в частности: 1) активация ренин-ангиотензиновой системы. Этот эффект связан с непосредственным действием катехоламинов на β-адренорецепторы юкстагломерулярного аппарата почек и опосредованным влиянием на ЮГА через спазм приносящих артериол; 2) внутрипочечное перераспределение кровотока. При активации симпатоадреналовой системы происходит спазм сосудов кортикальных нефронов. Вследствие этого основная часть крови идёт через юкстамедулярные нефроны, где площадь реабсорбции воды и ионов натрия, а также интенсивность этого процесса значительно больше, чем в кортикальных нефронах. Такое перераспределение кровотока в почках ведёт к значительному увеличению реабсорбции натрия и воды и способствует их сохранению в организме; 3) спазм артериол периферических тканей. При этом уменьшается фильтрация воды из капилляров в ткани, что способствует их сохранению в организме; 4) уменьшение потоотделения. Эта реакция направлена на уменьшение потери воды и солей организмом. При внеклеточном обезвоживании развиваются следующие защитно-компенсаторные реакции:
1. Происходит переход жидкости из интерстициального сектора в сосуды. Это связано с тем, что в условиях обезвоживания уменьшается гидростатическое давление крови в капиллярах, с одной стороны, и увеличивается онкотическое давление крови вследствие её сгущения (гемоконцентрации), с другой.
2. Уменьшение объёма циркулирующей крови, связанное с обезвоживанием, ведёт к возбуждению волюморецепторов и увеличению секреции антидиуретического гормона. Последний увеличивает реабсорбцию воды в почках, ограничивая её потерю организмом.
3. Уменьшение объёма циркулирующей крови вызывает активацию ренин-ангиотензивной системы и увеличение секреции альдостерона корой надпочечников. Это ведёт к увеличению реабсорбции ионов натрия в почках и к нормализации осмотического давления внеклеточной жидкости.
4. В результате уменьшения артериального давления возбуждаются барорецепторы, что приводит к активации симпатоадреналовой системы.
5. Обезвоживание через центральные и периферические механизмы вызывает чувство жажды. В результате формируются поведенческие реакции, направленные на поиск воды и восполнение потерянной жидкости.
Избыточное накопление воды в организмеВнеклеточная гипергидратация – это увеличение объёма жидкости во внеклеточном секторе организма. Она является результатом положительного водного баланса.
Причинами внеклеточной гипергидратации могут быть:
1. Избыточное поступление воды в организм: а) питьё солёной воды, не утоляющей жажду; б) внутривенное введение большого количества жидкости больным.
2. Задержка воды в организме вследствие нарушения её выделения почками: а) почечная недостаточность; б) нарушения регуляции почек (первичный и вторичный гиперальдостеронизм, гиперпродукция антидиуретического гормона).
При изоосмолярной гипергидратации осмотическое давление внеклеточной жидкости не изменяется. Этот вид нарушений может наблюдаться в течение некоторого времени после введения избыточного количества изотонического раствора.
Гипоосмолярная гипергидратация (водное отравление) характеризуется уменьшением осмотического давления внеклеточной жидкости. Этот вид гипергидратации в эксперименте на животных моделируют повторными введениями воды в желудок на фоне введения вазопрессина, альдостерона или удаления надпочечников. В клинике водное отравление возможно при рефлекторной анурии, а также во второй стадии острой почечной недостаточности.
Гиперосмолярная гипергидратация характеризуется увеличением осмотического давления внеклеточной жидкости и может развиваться при употреблении для питья солёной морской воды.
При внеклеточной гипергидратации развиваются следующие защитно-компенсаторные реакции:
1. Внеклеточная гипергидратация сопровождается увеличением объёма циркулирующей крови. Это ведёт к механическому растяжению клеток предсердий, которые в ответ освобождают в кровь предсердный натрийурический гормон. Последний увеличивает натрийурез и диурез, вследствие чего уменьшается объём циркулирующей крови.
2. Увеличение объёма циркулирующей крови является причиной уменьшения импульсации от волюморецепторов, в результате чего уменьшается секреция антидиуретического гормона и возрастает диурез.
Избыточное количество жидкости обычно не задерживается в крови, а переходит в ткани, прежде всего во внеклеточную среду, что приводит к развитию скрытых и явных отёков.
Почки относятся к жизненно важным органам. Основное назначение почек - сохранение постоянства внутренней среды (гомеостаза) организма:
1) поддержание на постоянном уровне объема внеклеточной жидкости и ее осмолярности путем влияния на размер экскреции воды и натрия;
2) регуляция содержания во внеклеточной жидкости калия, магния, кальция, фосфора, хлора и других электролитов;
3) участие в поддержании на нормальном уровне рН крови путем задержки в организме, удаления и продукции кислых и щелочных субстанций;
4) удаление из плазмы крови токсических и конечных продуктов обмена, избытка глюкозы, аминокислот, пептидов и полипептидов, в том числе различных гормонов, а также чужеродных веществ (лекарственные препараты, яды и пр.);
5) участие в регуляции кровяного давления и эритропоэза.
Значительная часть перечисленных функций связана с экскреторной деятельностью почек, суммарным результатом которой является образование мочи.
Используемая литература:
1. Бышевский А. Ш., Терсенов О. А. Биохимия для врача // Екатеринбург: Уральский рабочий, 1994, 384 с.;
2. Ленинджер А. Биохимия. Молекулярные основы структуры и функций клетки // М.: Мир, 1974, 956 с.;
3. Пустовалова Л.М. Практикум по биохимии // Ростов-на Дону: Феникс, 1999, 540 с.;













 (zip - application/zip)
(zip - application/zip)