Хлори́д серебра́(I) (хлористое серебро) — AgCl
Хлорид таллия — бинарное неорганическое соединение, соль металла таллия и соляной кислоты с формулой TlCl, бесцветные кристаллы, плохо растворимые в воде.
Окси́д ме́ди(II) (окись меди) CuO — основный оксид двухвалентной меди.
Oксид кремния (IV) (диоксид кремния, кремнезём SiO2)
Окси́д бо́ра B2O3 — ангидрид борной кислоты,
Хлори́д ме́ди(I) CuСl— бинарное химическое соединение, медная соль хлороводородной кислоты.
Хлорид таллия — бинарное неорганическое соединение, соль металла таллия и соляной кислоты с формулой TlCl
Окси́д на́трия — бинарное неорганическое вещество, имеющее формулу Na2O
Br (лат. Bromum). оксиды сурьмы Sb2O3, SnO оксид олова
Оксид церия(IV), диоксид церия, двуокись церия — химическое соединение церия и кислорода с формулой CeO2
Обычно как в стекле, так и в кристаллическом кварце каждый атом кислорода, соединенный с двумя атомами кремния, называется мости-ковым. В кварцевом стекле некоторые атомы кислорода соединены только с одним атомом кремния; такие атомы кислорода называются немостиковыми.
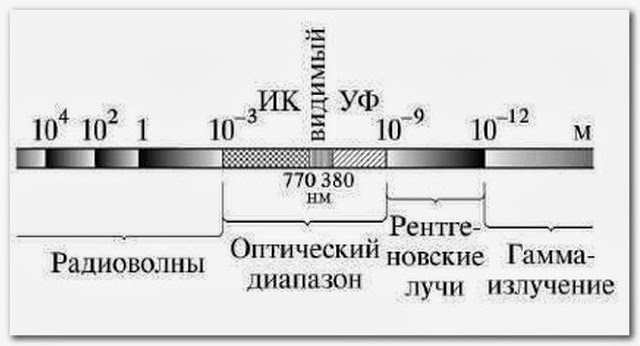
Це́нтры окра́ски (ЦО) — точечные дефекты в прозрачных диэлектриках (кристаллах и стёклах), поглощающие оптическое излучение вне области собственного поглощения диэлектрика, то есть в той спектральной области, где поглощение бездефектного диэлектрика отсутствует и он вследствие этого прозрачен.
Фотодиссоциация (или фотолиз) — химическая реакция, при которой химические соединения разлагаются под действием фотонов электромагнитного излучения.
Для этого процесса принципиальное значение имеет так называемая энергия активации — свойство участвующей в процессе молекулы — и превышение этой энергии энергией взаимодействующего фотона.
Силикаты и алюмосиликаты представляют собой обширную группу минералов. Для них характерен сложный химический состав и изоморфные замещения одних элементов и комплексов элементов другими. Главными химическими элементами, входящими в состав силикатов, являются Si, O, Al, Fe2+, Fe3+, Mg, Mn, Ca, Na, K, а также Li, B, Be, Zr, Ti, F, H, в виде (OH)− или H2O и др.
Галогени́ды (галоиды) — соединения галогенов с другими химическими элементами или радикалами. При этом галоген, входящий в соединение, должен быть электроотрицательным; так, оксид брома не является галогенидом.По участвующему в соединении галогену галогениды также называются фторидами, хлоридами, бромидами, иодидами и астатидами. Наиболее известны под этим названием галогениды серебра благодаря массовому распространению плёночной галогеносеребряной фотографии.Соединения галогенов между собой называются интергалогенидами, или межгалоидными соединениями (например, пентафторид иода IF5).В галогенидах галоген имеет отрицательную степень окисления, а элемент — положительную.
Галогениды — группа минералов, представляющих собой соединения галогенов с другими химическими элементами или радикалами.К галогенидным минералам относятся фтористые, хлористые и очень редкие бромистые и иодистые соединения. Фтористые соединения (фториды), генетически связаны с магматической деятельностью, они являются возгонами вулканов или продуктами гидротермальных процессов, иногда имеют осадочное происхождение.Галогенидные минералы являются oсадками морей и озёр и главными минералами соляных толщ и месторождений. Некоторые галогенные соединения образуются в зоне окисления сульфидных (медных, свинцовых и других) месторождений.К практически важным фторидам и хлоридам можно отнести: флюорит (плавиковый шпат), галит (поваренная соль), сильвин, карналлит.
Сущность спектральной сенсибилизации заключается в том, что кванты света, непосредственно не поглощаемые микрокристаллами галогенидов серебра, поглощаются красителем при экспонировании и при этом энергия фотовозбуждённых молекул красителя передается кристаллам галогенида серебра, образуя в них скрытое изображение, которое затем проявляется фотографическим проявителем.
Сенсибилиза́тор — вещества, вводимые в фотослой.
· Химические сенсибилизаторы, например, комплексные соли золота и некоторые сернистые соединения вводят в фотографическую эмульсию при её изготовлении и приводят к более интенсивному образованию центров светочувствительности на микрокристаллах галогенидов серебра. Это приводит к росту естественной светочувствительности фотоматериала в сине-фиолетовой области.
· Оптические сенсибилизаторы (циановые красители, флуоресцентные отбеливатели) вводятся перед поливкой готовой фотоэмульсии на подложку. Они взаимодействуют с ионами серебра на поверхности микрокристалла. Это обеспечивает дополнительную чувствительность в разных областях спектра.
Ши́хта (нем. Schicht) — смесь исходных материалов, а в некоторых случаях (например, при выплавке чугуна в доменной печи) и топлива в определённой пропорции, подлежащая переработке в металлургических, химических и других агрегатах.
Шихтами обычно называют исходные смеси, использующиеся в пирометаллургических или иных высокотемпературных процессах (производство стекла, цемента, некоторых керамических материалов и изделий, коксование углей).
В состав металлургических шихт обычно входят исходное или обогащённое рудное сырьё, сырьё с флюсами и оборотными материалами. Шихты в чёрной металлургии (например, в доменном процессе) зачастую содержат и топливо, в то время как в цветной металлургии шихты, как правило, топлива не содержат.
Типичные требования к качеству шихты определяются обеспечением стабильности и воспроизводимости результатов процесса, в котором она используется:
· постоянство химического состава;
· однородность по химическому, минералогическому и гранулометрическому составу;
· оптимальная крупность компонентов шихты;
· оптимальная влажность.
Анизотропи́я (от др.-греч. ἄνισος — неравный и τρόπος — направление) — различие свойств среды (например, физических: упругости, электропроводности, теплопроводности, показателя преломления, скорости звука или света и др.) в различных направлениях внутри этой среды; в противоположность изотропии.
В отношении одних свойств среда может быть изотропна, а в отношении других — анизотропна; степень анизотропии также может различаться.
Частный случай анизотропии — ортотропия (от др.-греч. ὀρθός — прямой и τρόπος — направление) — неодинаковость свойств среды по взаимно перпендикулярным направлениям.
Коллоидные системы, коллоиды (др.-греч. κόλλα — клей + εἶδος — вид; «клеевидные») — дисперсные системы, промежуточные между истинными растворами и грубодисперсными системами — взвесями, в которых дискретные частицы, капли или пузырьки дисперсной фазы, имеющие размер хотя бы в одном из измерений от 1 до 100 нм, распределены в дисперсионной среде, обычно непрерывной, отличающейся от первой по составу или агрегатному состоянию. В свободнодисперсных коллоидных системах (дымы,золи) частицы не выпадают в осадок.














 (zip - application/zip)
(zip - application/zip)